服务热线
010-57895631
发布时间:2022/11/7 9:05:00 发布人:mayi
2021年,国家药品监督管理局共批准创新医疗器械35个,比2020年增加35%。
2021年,国家药品监督管理局批准境内第三类医疗器械注册4596项,比2020年增加27.6%。批准进口医疗器械注册6718项,比2020年增加7.6%。
这都是技术审评制度改革的重要成果。2015年,国务院发布了一份《关于改革药品医疗器械审评审批制度的意见》,从而拉开了医疗器械审评审批制度的改革。2020年,在由中国欧盟商会主办的“后疫情时代的新常态――创新助力‘健康中国’第二届医疗器械论坛”上,审评中心的领导和专家就近两年审评改革的内容作了梳理与讲解。
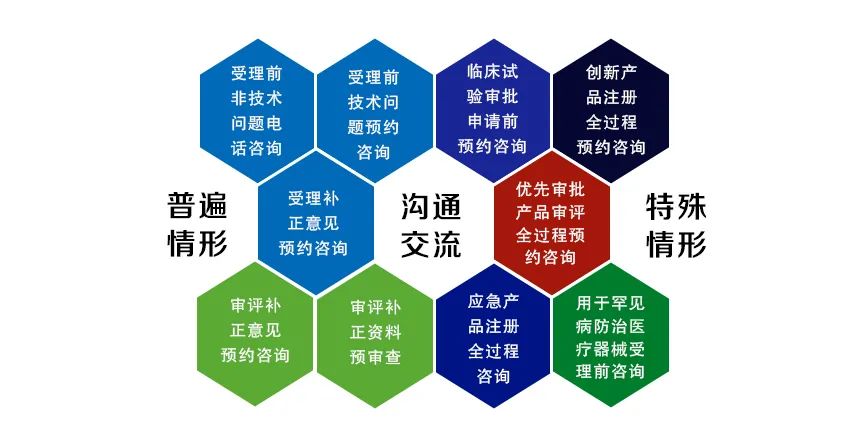
图片来源:审评专家演示PPT
作为医疗器械审评审批制度改革的见证者,迈迪思创也在时刻关注和研究法规制度的变化,为全球合作客户提供更专业、更高效的医疗器械产品中国上市前一站式法规咨询服务。目前,迈迪思创已拥有超过100名技术人员的专业团队,主要成员为一流跨国企业、国内生产企业、法规咨询机构的注册、临床、质量管理体系与生产管理一线精英。在10年的创新发展历程中,迈迪思创协助全球数百家医疗器械制造商,取得进口与国产医疗器械注册证书1500多张。临床试验研究服务优势领域扩展至多个医疗器械前沿科学,包括手术导航定位系统、AI人工智能辅助诊断、医疗影像设备、创新生物医用材料、骨科植入器械、医疗美容设备与植入剂、体外诊断试剂等。


